Oxido de nitrato – conceito
tabela periódica
Óxido de nitrato é um conjunto de compostos químicos formados por óxidos (oxigénio) que reagem com o nitrato formando diferentes estruturas, como por exemplo o óxido nítrico e o óxido nitroso.
Estes óxidos possuem propriedades que afetam o ser humano, tanto a nível positivo, como a nível negativo. Em alguns casos estes óxidos fazem de intermediários entre as substâncias presentes nas células, enquanto outros óxidos de nitrato ao serem libertados para a atmosfera podem ser responsáveis pelo aquecimento global.
Oxido nítrico
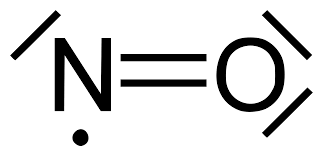
oxido nítrico
Este oxido trata-se de uma molécula simples, que também pode ser designada por monóxido de nitrogénio, pois a molécula é formada por um átomo oxigénio e um átomo azoto (nitrogénio), podendo por isso designar-se ainda por monóxido de azoto ou monóxido de nitrogénio.
Este trata-se de um gás incolor que se encontra em pequenas quantidades na atmosfera, no entanto, sendo produzido em seres vivos, a sua libertação para a atmosfera leva a uma rápida oxidação do oxido tornando-o num gás de cor acastanhada. A sua concentração pode torna-lo num gás benéfico ou num gás tóxico para os organismos.
O oxido nítrico é capaz de se dissolver em diversos tipos de lípidos, como gorduras e óleos vegetais. Os óxidos de nitrato, particularmente o oxido nítrico atua nas paredes dos vasos sanguíneos, tornando-as mais flexíveis, o que contribui para o aumento da sua dimensão e consequentemente o aumento do fluxo sanguíneo, favorecendo o seu uso no tratamento de doenças coronárias, pois dilata as artérias coronárias, aumentando a sua irrigação. Quando produzido no próprio organismo o oxido de nitrato tem a capacidade de agir como elemento de defesa do organismo, podendo ainda atuar como neurotransmissor.
Este gás é muito reativo, criando facilmente radicais livres que interagem com as moléculas existentes na atmosfera, tornando-o altamente tóxico, quando em quantidades elevadas. Este oxido apresenta efeitos semelhantes ao monóxido de carbono, possuindo uma toxicidade que leva ao aumento da corrosibilidade do ar, provocando danos tanto ao nível material, assim como a nível da saúde da população.
O oxido nítrico ao ser libertado para a atmosfera, através de vários meios, vai interagir com os componentes formando acido nítrico, que corresponde a um dos principais elementos que compõem as chuvas acidas, ou forma um nevoeiro denso e tóxico designado geralmente pelo termo smog fotoquímico.
Oxido nitroso:
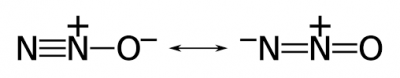
oxido nitroso
Outro tipo de oxido de nitrato é o oxido nitroso, um composto químico formado por um átomo de oxigénio e dois átomos de azoto ou nitrogénio, representado pela formula N2O. Este é naturalmente emitido por bactérias que existem no solo, no entanto, as principais atividades produtoras deste gás são a agricultura, a produção de gado, assim como as produções industriais e os gases produzidos pelo escape dos carros.
Apesar de se encontrar naturalmente presente na atmosfera, em pequenas quantidades, estes gás corresponde a um dos gases mais emitidos e consequente mais prejudiciais para a camada de ozono, comparável muitas vezes com os CFCs, pois tem uma elevada capacidade de captação dos raios ultravioleta e consequentemente do calor, aumentando assim o efeito de estufa e o aquecimento global.
O Oxido Nitroso, um dos óxidos de nitrato que se encontra envolvido no ciclo do nitrogénio, mantém-se na atmosfera por mais de 100 anos acabando por ser degradado ao longo do ciclo de nitrogénio e preso no solo devido ao efeito das plantas. No entanto, quando em grandes quantidades o ciclo de nitrogénio não consegue absorver todo o oxido nitroso presente na atmosfera, levando a que este interajam com outras substancias criando ácidos que se podem tornar prejudiciais ao ambiente, assim como as seres vivos.
Este gás é conhecido como o gás do riso, pois a sua ingestão provoca euforia, assim como ligeiras alucinações. Em condições ambientais normais, trata-se de um gás sem cor, sem cheiro,não é inflamável, nem tóxico e pode apresentar um sabor metálico.
O gás é utilizado particularmente na medicina, onde é usado como anestésico, é ainda utilizado em combustíveis aumentando o poder do motor, tendo sido usado em alguns foguetões espaciais.
References:
Flora Filho, R., & Zilberstein, B.. (2000). Óxido nítrico: o simples mensageiro percorrendo a complexidade. Metabolismo, síntese e funções. Revista da Associação Médica Brasileira, 46(3), 265-271. Consultado em: Maio 31, 2018, em www.scielo.br/scielo.php?script=sci_arttext&pid=S0104-42302000000300012
Overview of Greenhouse Gases. Greenhouse Gas Emissions. Climate Change Division. Office of Atmospheric Programs (MC-6202A). U.S. Environmental Protection Agency. Consultado em: Maio 31, 2018, em https://www.epa.gov/ghgemissions/overview-greenhouse-gases
Zumdahl, Steven S. (2018). Oxide. Encyclopædia Britannica, inc. Consultado em: Maio 31, 2018, em https://www.britannica.com/science/oxide/Nonmetal-oxides#ref278021
(2017) Nitric oxide. Encyclopædia Britannica, inc. Consultado em: Maio 31, 2018, em https://www.britannica.com/science/nitric-oxide





